では、なぜ原子がある特定の波長の光を吸収するのか考えてみましょう。
原子は、基底状態より励起状態へ遷移するときにある特定波長の光を吸収し、その励起状態から基底状態へ遷移するときに発熱或いは発光します。この発光スペクトルは、原子スペクトルといい線スペクトルです。これらのスペクトルは、2つのエネルギー準位
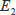
,
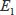
間の遷移により生じます。例えば水素の場合には、
で表されます。
ここで、
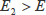
また
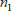
、
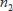
は量子数(正の整数)で
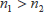
,
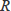
はRydberg定数と呼び、109737cm-1です。多電子原子の場合には、主量子数

の他に、全軌道量子数
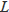
、全スピン量子数
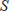
、全内部量子数
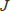
が加わりスペクトルはより複雑となります。スペクトル線を生じるエネルギー遷移の様子を図に示したものをグロトリアン図といいます。(図4・2)ナトリウムの2本のD線は、589.59nm及び588.99nmのスペクトル線に相当します。
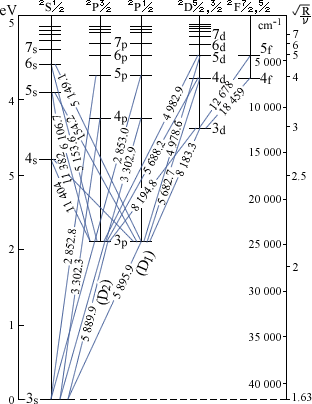
図4・2 ナトリウム原子のグロトリアン図
